
Glicerol
| Glicerol Alerta sobre risco à saúde | |
|---|---|
| |

| |

| |
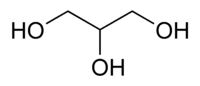
| Nome IUPAC | Propano-1,2,3-triol |
| Nome sistemático | Glicerol |
| Outros nomes | Glicerina |
| Identificadores | |
| Abreviação | Gro |
| Número CAS | 56-81-5 |
| PubChem | 3416 |
| Número EINECS | 200-289-5 |
| KEGG | CE00116 |
| MeSH | D005990 |
| ChEBI | 17754 |
| Número RTECS | MA8050000 |
| Código ATC | A06AG04 |
| SMILES |
|
| InChI |
1/C3H8O3/c4-1-3(6)2-5/h3-6H,1-2H2
|
| Referência Beilstein | 4-01-00-02751 |
| 3DMet | B00032 |
| Propriedades | |
| Fórmula química | C3H8O3 |
| Massa molar | 92.0776 g mol-1 |
| Aparência | Líquido incolor |
| Odor | Inodoro |
| Densidade | 1,2613 g cm–3 (20 °C) |
| Ponto de fusão |
18.1 °C, 291 K, 65 °F |
| Ponto de ebulição |
290 °C, 563 K, 554 °F |
| Solubilidade em água | Miscível |
| Solubilidade em etanol | Miscível |
| Solubilidade em éter | Levemente solúvel |
| Solubilidade em benzeno | Insolúvel |
| Solubilidade em tetracloreto de carbono | Insolúvel |
| Solubilidade em triclorometano | Insolúvel |
| log P | -1,671 |
| Pressão de vapor | 0,33 Pa (50 °C) 26 Pa (100 °C) 573 Pa (150 °C) 6100 Pa (200 °C) |
| kH | 1,73 |
| Atmospheric OH rate constant | 1,87 × 10-11 |
| Acidez (pKa) | 14,4 |
| Basicidade (pKb) | -0,4 |
| λmax | < 207 nm |
| Condutividade térmica | 0,285 W m-1 K-1 (25 °C) 0,288 W m-1 K-1 (50 °C) 0,292 W m-1 K-1 (75 °C) 0,296 W m-1 K-1 (100 °C) |
| Índice de refracção (nD) | 1,4746 (20°C, 589 nm) |
| Viscosidade | 1,5 Pa s (20 °C) 934 mPa s (25 °C) 152 mPa s (50 °C) 39,8 mPa s (75 °C) 14,8 mPa s (100 °C) |
| Momento dipolar | 0,9613587967 D |
| Estrutura | |
| Estrutura cristalina | Xarope, ortorômbico, lamelar |
| Forma molecular | sp3 |
| Termoquímica | |
|
Entalpia padrão de formação ΔfH |
−669,6 kJ mol-1 (líquido) −577,9 kJ mol-1 (gás) |
|
Entalpia padrão de combustão ΔcH |
1 655,4 kJ mol-1 |
|
Entropia molar padrão S |
206,3 J mol-1 K-1 |
|
Capacidade calorífica molar Cp298 |
218,8 J mol-1 K-1 |
| Farmacologia | |
| Riscos associados | |
| MSDS | ScienceLab.com |
| NFPA 704 | |
| Ponto de fulgor | 160 °C Fechado 177 °C Cleveland 199 °C Pensky-Martens 204 °C Ponto de ignição |
| Compostos relacionados | |
| Outros aniões/ânions | 3-cloro-1,2-propanodiol |
| Polióis e açúcares relacionados |
Etilenoglicol Propilenoglicol Propano-1,3-diol Eritritol (butano-1,2,3,4-tetraol) Gliceraldeído |
| Compostos relacionados |
Glicerol-3-fosfato Triacilgliceróis (ésteres) |
| Página de dados suplementares | |
| Estrutura e propriedades | n, εr, etc. |
| Dados termodinâmicos | Phase behaviour Solid, liquid, gas |
| Dados espectrais | UV, IV, RMN, EM |
|
Exceto onde denotado, os dados referem-se a materiais sob condições normais de temperatura e pressão Referências e avisos gerais sobre esta caixa. Alerta sobre risco à saúde. | |
Glicerol ou propanotriol (IUPAC, 1993) é um composto orgânico pertencente à função álcool. É líquido à temperatura ambiente (25 °C), higroscópico, inodoro, viscoso e de sabor adocicado. O nome origina-se da palavra grega glykós (γλυκός), que significa "doce". O termo glicerina refere-se ao produto na forma comercial, com pureza acima de 95%.
Ocorrência
O glicerol está presente em todos os óleos e gorduras de origem animal e vegetal em sua forma combinada, ou seja, ligado a ácidos graxos tais como o ácido esteárico, oleico, palmítico e láurico para formar a molécula de triacilglicerol.
Os óleos de coco e de palma (óleo de dendê) contêm uma alta quantidade (70% a 80%) de ácidos graxos com cadeia carbônica de 6 a 14 carbonos. Estes rendem muito mais glicerol do que os óleos contendo ácidos graxos de 16 a 18 carbonos, tais como gorduras, óleo de algodão, soja, oliva e palma. O glicerol combinado está presente também em todas as células animais e vegetais, fazendo parte de sua membrana celular, na forma de fosfolipídios.
Produção de Glicerol
Todo o glicerol produzido no mundo, até 1949, era proveniente da indústria de sabão. Atualmente, 70% da produção de glicerol nos Estados Unidos ainda provém dos glicerídeos (óleos e gorduras naturais) e, o restante, da produção do glicerol sintético (subproduto da fabricação de propileno), da produção de ácidos graxos e também como subproduto da transesterificação de ésteres, onde é substituída como álcool ligado aos de ácidos graxos pelo metanol ou etanol, resultando em biodiesel.
Em 2000, a produção mundial de glicerol foi de 800 mil toneladas, sendo que 10% disto foram oriundos de indústrias responsáveis pela produção de Biodiesel.
Aplicações
Saúde e fatores de risco
O glicerol é reconhecido como seguro para o consumo humano desde 1959, podendo ser utilizado em diversos produtos alimentícios para os mais diversos propósitos. Os níveis de DL50 em ratos são de 470 mg/kg e em porquinhos-da-índia de 7750 mg/kg. Vários estudos mostraram que uma grande quantidade de glicerol (sintético ou natural) pode ser administrada sem aparecimento de qualquer efeito adverso à saúde.
Alimentos e bebidas
É frequentemente utilizado como/em. Entre eles:
- umectante, solvente, amaciante;
- umectante e agente suavizante em doces, bolos e sorvetes, retardando a cristalização do açúcar;
- agente umectante nas embalagens de queijos e carnes;
- solvente e agregador de consistência em flavorizantes e corantes;
- produção de mono–, di–, ou triglicerídeos para uso em emulsificantes;
- produção de polímeros, como poliglicerol, que são adicionados em margarinas (E475 e E476);
- meio facilitador da transferência de calor, por estar em contato direto com o alimento, permitindo que algum alimento específico seja rapidamente resfriado para que não perca algumas características desejáveis.
- é o principal componente do e-liquid (líquido usado nos cigarros eletrônicos).
Uma colher de chá de glicerol tem aproximadamente 27 kcal e tem um poder adoçante equivalente a 60% da sacarose (açúcar de cana). Embora o glicerol apresente aproximadamente o mesmo nível energético obtido pelo açúcar comum, ele não eleva os níveis de açúcar no sangue (veja glicemia) e também não alimenta as bactérias que causam a cárie. Em sua forma concentrada ele jamais deve ser consumido, pois ocasiona a retirada de água dos tecidos vivos causando problemas gástricos. Como aditivo alimentar, ele é reconhecido pelo número E - E422, pertencendo à classe dos espessantes, estabilizadores, gelificantes e emulsionantes. Quando presente em alimentos, ele é facilmente digerido como se fosse um carboidrato.
Medicamentos
Na área médica/hospitalar/farmacêutica há inúmeros produtos que utilizam o glicerol. Entre eles:
- Pomadas;
- Elixires, xaropes;
- Anestésicos;
- Seus derivados são utilizados como tranquilizantes e agentes para controle da pressão, como a nitroglicerina, que é um importante vasodilatador;
- Em cosméticos ele entra em muitos cremes e loções que mantém a maciez e umidade da pele;
- Em cremes dentais, é comum ser utilizado para conferir-lhe brilho, suavidade e viscosidade.
Outras aplicações
- Na indústria de resina o glicerol é usado na produção de resinas. O grupo hidróxido deste álcool reage com o grupo carboxílico dos ácidos resínicos formando um éster de glicerina (éster de colofónia). Estes ésteres são cada vez mais utilizados no fabrico de adesivos;
- Na produção de tabaco. Entre eles:, quando as folhas são quebradas e empacotadas, o glicerol é pulverizado impedindo que as mesmas se tornem secas e quebradiças, o que poderia ocasionar o esfarelamento;
- Na indústria têxtil é utilizado para amaciar e flexibilizar as fibras;
- O glicerol é utilizado também na indústria de papel na fabricação de alguns papéis especiais, que necessitam de alguns agentes plastificantes para conferir-lhes maleabilidade e tenacidade;
- Pode ser utilizado como lubrificante em máquinas que fabricam produtos alimentícios, que entram em contato direto com o alimento ou, quando existir qualquer tipo de incompatibilidade com os produtos utilizados no processo, tais como em rolamentos expostos a solventes como gasolina ou benzina, que poderiam dissolver o óleo mineral;
- Utilizado em misturas anticongelantes;
- Utilizado para preservar bactérias a temperaturas baixas.
- combustível.
- Existem algumas formas de utilização para hidratação caseira com glicerina no cabelo.
Bibliografia
- "Guia IUPAC para a Nomenclatura de Compostos Orgânicos" Tradução Portuguesa na variantes Europeia e Brasileira de "A Guide to IUPAC Nomenclature of Organic Compounds - Recomendations 1993", original em inglês preparado por R. Pânico, W. H. Powell e J.-C. Richer.
- JUNGERMANN, E.; SONNTAG, N. O. V. Glycerine: a key cosmetic ingredient. New York: Marcel Dekker, 1991. 460 p. (Cosmetic science and technology series, 11).
- KIRK-OTHMER, E. T. Glycerol. In: American Society of Chemistry. Encyclopedia of chemical technology. 5. ed. New York: John Wiley, 2007. Disponível em: Wiley.com. Acesso em: 12 maio 2007.
- LIDE, David R. (Ed.), TAYLOR and FRANCIS. CRC Handbook of Chemistry and Physics. 89.ed (Internet version 2007). Boca Raton, FL. Disponível em: HBCPnetbase. Acesso em: 14 mar. 2009.
Ligações externas
- «Absolute alcohol using glycerol»
- «Computational Chemistry Wiki»
- «Glycerol on BioChemInfo.org»
- «Physical Property of glycerol»
|
Tipos de lípidos
| |
|---|---|
| Geral | |
| Ácidos gordos | |
| (Acil)glicerídeos | |
| Ceras | |
| Fosfoglicéridos | |
| Esfingolípidos | |
| Glicolípidos | |
| Esteróides | |
| Terpenos | |
| Eicosanoides | |
| Componentes | |
