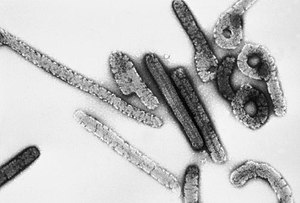
Doença do vírus de Marburg
|
Doença do vírus de Marburg (febre hemorrágica de Marburg) | |
|---|---|
| Eletromicrografia de transmissão do vírus de Marburg | |
| Especialidade | Doenças infecciosas |
| Sintomas | Febre, fraqueza, dor muscular |
| Duração | 2–21 dias após a exposição |
| Causas | Vírus de Marburg |
| Fatores de risco | Contato direto com fluidos corporais de indivíduos infectados pelo vírus |
| Método de diagnóstico | Teste de sangue |
| Condições semelhantes | Doença por vírus Ébola |
| Tratamento | Não há tratamento, apenas cuidados de suporte imediatos |
| Frequência | Rara |
| Mortes | Taxa de letalidade de 24%–88% |
| Classificação e recursos externos | |
| CID-10 | A98.3 |
| CID-9 | 078.89 |
| CID-11 | 696598707, 510498140 |
| DiseasesDB | 4033 |
| eMedicine | 969877 |
| MeSH | D008379 |
|
| |
A doença do vírus de Marburg (MVD do inglês: Marburg virus disease; anteriormente conhecida como febre hemorrágica de Marburg) é uma febre hemorrágica viral em primatas humanos e não humanos, causada por um dos dois vírus de Marburg: vírus de Marburg (MARV) e vírus de Ravn (RAVV). Seus sintomas clínicos são muito semelhantes aos da doença por vírus Ébola (DVE).
Acredita-se que os morcegos frugívoros egípcios sejam os portadores normais na natureza e o RNA do vírus de Marburg foi isolado deles.
Sinais e sintomas
O estudo mais detalhado sobre a frequência, início e duração dos sinais e sintomas clínicos da MVD foi realizado durante o surto misto da doença MARV/RAVV de 1998–2000. Uma erupção maculopapular, petéquias, púrpura, equimoses e hematomas (especialmente ao redor dos locais de injeção da agulha) são manifestações hemorrágicas típicas. No entanto, ao contrário da crença popular, a hemorragia não leva à hipovolemia e não é a causa da morte (a perda total de sangue é mínima, exceto durante o parto). Em vez disso, a morte ocorre devido à síndrome da disfunção de múltiplos órgãos devido à redistribuição de fluidos, hipotensão, coagulação intravascular disseminada e necroses teciduais focais.
As fases clínicas da apresentação da febre hemorrágica de Marburg (MHF) são descritas a seguir. Observe que as fases se sobrepõem devido à variabilidade entre os casos:
- Fase de Incubação: 2 a 21 dias, com média de 5 a 9 dias.
- Fase de Generalização: Dia 1 até o Dia 5 desde o início dos sintomas clínicos. A MHF se apresenta com febre alta de cerca de 40ºC e uma dor de cabeça súbita e intensa, acompanhada de calafrios, fadiga, náusea, vômito, diarreia, faringite, erupção cutânea maculopapular, dor abdominal, conjuntivite e mal-estar.
- Fase Inicial do Órgão: Dia 5 até o Dia 13. Os sintomas incluem prostração, dispneia, edema, hiperemia conjuntival, exantema viral e sintomas do sistema nervoso central, incluindo encefalite, confusão, delírio, apatia e agressividade. Os sintomas hemorrágicos geralmente ocorrem tardiamente e anunciam o fim da fase inicial do órgão, levando a uma eventual recuperação ou piora e morte. Os sintomas incluem fezes com sangue, equimoses, vazamento de sangue de locais de punção venosa, hemorragia visceral e mucosa e, possivelmente, hematemese.
- Fase Terminal do Órgão: dia 13 até dia 21+. Os sintomas se bifurcam em duas constelações: ou para sobreviventes ou para casos fatais. Os sobreviventes entrarão em uma fase de convalescença, experimentando mialgia, fibromialgia, hepatite, astenia, sintomas oculares e psicose. Os casos fatais continuam a piorar, apresentando febre contínua, obnubilação, coma, convulsões, coagulopatia difusa, distúrbios metabólicos, choque e morte, com a morte ocorrendo tipicamente entre os dias 8 e 16.
Causas
| Nome da espécie | Nome do vírus (abreviação) |
| Marburg marburgvirus* | Vírus de Marburg (MARV; anteriormente MBGV) |
| Vírus de Ravn (RAVV; anteriormente MARV-Ravn) | |
| * = denota a espécie-tipo. | |
A MVD é causada por dois vírus: vírus de Marburg (MARV) e vírus de Ravn (RAVV), ambos da família Filoviridae.
Os marburgvirus são endêmicos em florestas áridas da África Equatorial. A maioria das infecções por marburgvirus foi repetidamente associada a pessoas que visitavam cavernas naturais ou trabalhavam em minas. Em 2009, o isolamento bem-sucedido do MARV e RAVV infecciosos foi relatado em morcegos frugívoros egípcios saudáveis capturados em cavernas. Esse isolamento sugere fortemente que os morcegos frugívoros do Velho Mundo estão envolvidos na manutenção natural dos marburgvirus, e que visitar cavernas infestadas por morcegos é um fator de risco para adquirir infecções por marburgvirus. Porém, mais estudos são necessários para estabelecer se os morcegos egípcios são os verdadeiros hospedeiros do MARV e RAVV ou se eles são infectados por contato com outro animal e, portanto, servem apenas como hospedeiros intermediários. Outro fator de risco é o contato com primatas não humanos, embora apenas um surto de MVD (em 1967) tenha ocorrido devido ao contato com macacos infectados.
Ao contrário da doença por vírus Ébola (DVE), que tem sido associada a fortes chuvas após longos períodos de tempo seco, os fatores desencadeantes para o transbordamento do vírus de Marburg na população humana ainda não foram descritos.
Diagnóstico
A MVD é clinicamente indistinguível da doença por vírus Ébola (DVE) e também pode ser facilmente confundida com muitas outras doenças prevalentes na África Equatorial, como outras febres hemorrágicas virais, malária falciparum, febre tifoide, shigelose, doenças rickettsiais como tifo, cólera, sepse gram-negativa, borreliose, como febre recorrente ou enterite por EHEC. Outras doenças infecciosas que devem ser incluídas no diagnóstico diferencial incluem leptospirose, tifo esfolioso, peste, febre Q, candidíase, histoplasmose, tripanossomíase, leishmaniose visceral, varíola hemorrágica, sarampo e hepatite viral fulminante. Doenças não infecciosas que podem ser confundidas com a MVD são leucemia promielocítica aguda, síndrome hemolítico-urêmica, envenenamento por cobra, deficiências de fator de coagulação/distúrbios plaquetários, púrpura trombocitopênica trombótica, telangiectasia hemorrágica hereditária, síndrome de Kawasaki e até intoxicação por varfarina. O indicador mais importante que pode levar à suspeita da MVD no exame clínico é a história médica do paciente, em particular a história de viagens e a história ocupacional (que países e cavernas foram visitadas?) e a exposição do paciente à vida selvagem (exposição a morcegos ou excrementos de morcegos?). A MVD pode ser confirmada pelo isolamento do vírus de Marburg ou pela detecção do antígeno do vírus de Marburg ou RNAs genômicos ou subgenômicos em amostras de sangue ou soro do paciente durante a fase aguda da MVD. O isolamento do Marburgvirus geralmente é realizado pela inoculação de culturas de células epiteliais Vero E6 ou MA-104 do rim de Chlorocebus aethiops ou pela inoculação de células SW-13 do carcinoma adrenal humano, todas as quais reagem à infecção com efeitos citopáticos característicos. Os filovirions podem ser facilmente visualizados e identificados na cultura celular por eletromicrografia devido às suas formas filamentosas únicas, porém, a eletromicrografia não pode diferenciar os vários filovírus sozinhos, apesar de algumas diferenças gerais de comprimento. Ensaios de imunofluorescência são usados para confirmar a presença do Marburgvirus em culturas celulares. Durante um surto, o isolamento do vírus e a eletromicrografia geralmente não são opções viáveis. Os métodos de diagnóstico mais comuns são, portanto, RT-PCR em conjunto com ELISA de captura de antígeno, que pode ser realizado em hospitais e laboratórios de campo ou móvel. Ensaios de imunofluorescência indireta não são mais usados para diagnóstico da MVD no campo.
Classificação
A doença do vírus de Marburg (MVD) é o nome oficial listado na Classificação Estatística Internacional de Doenças e Problemas Relacionados com a Saúde 10 (CID-10) da Organização Mundial da Saúde para a doença humana causada por qualquer um dos dois Marburgvirus: vírus de Marburg (MARV) e vírus de Ravn (RAVV). Na literatura científica, a febre hemorrágica de Marburg (MHF) é frequentemente usada como um nome alternativo não oficial para a mesma doença. Ambos os nomes das doenças são derivados da cidade alemã de Marburg, onde o MARV foi descoberto pela primeira vez.
Transmissão
Os detalhes da transmissão inicial da MVD para humanos permanecem incompletos. A transmissão provavelmente ocorre de morcegos frugívoros egípcios ou outro hospedeiro natural, como primatas não humanos ou através do consumo de carne de animal silvestre, mas as vias específicas e os fluidos corporais envolvidos são desconhecidos. A transmissão da MVD entre humanos ocorre por meio do contato direto com fluidos corporais infectados, como o sangue.
Prevenção
Atualmente, não há vacinas aprovadas pela Food and Drug Administration para a prevenção da MVD. Muitas vacinas candidatas foram desenvolvidas e testadas em vários modelos animais. Dessas, as mais promissoras são as vacinas de DNA ou baseadas em replicons do vírus da encefalite equina venezuelana, do vírus da estomatite vesicular ou de partículas semelhantes ao filovírus, sendo que todos esses candidatos poderiam proteger primatas não humanos da doença induzida pelo vírus de Marburg. Vacinas de DNA entraram em ensaios clínicos.Marburgviruses são altamente infecciosos, mas não muito contagiosos. Eles não são transmitidos por aerossol durante surtos naturais da MVD. Devido à ausência de uma vacina aprovada, a prevenção da MVD depende predominantemente da quarentena de casos confirmados ou de alta probabilidade, equipamento de proteção individual adequado, esterilização e desinfecção.
Zonas endêmicas
Os hospedeiros naturais de manutenção dos vírus de Marburg ainda precisam ser identificados de forma inequívoca. No entanto, o isolamento da MARV e RAVV de morcegos, e a associação de vários surtos da MVD com minas ou cavernas infestadas por morcegos, sugere fortemente que os morcegos estão envolvidos na transmissão do vírus de Marburg para humanos. Evitar o contato com morcegos e abster-se de visitas a cavernas é altamente recomendado, mas pode não ser possível para aqueles que trabalham em minas ou pessoas que dependem de morcegos como fonte de alimento.
Durante surtos
Como os vírus de Marburg não são transmitidos por aerossol, o método de prevenção mais direto durante os surtos da MVD é evitar o contato direto (pele a pele) com os pacientes, suas excreções e fluidos corporais e quaisquer materiais e utensílios possivelmente contaminados. Os pacientes devem ser isolados, mas ainda estão seguros para serem visitados por familiares. A equipe médica deve ser treinada e aplicar técnicas rígidas de enfermagem de bloqueio do vírus (máscara facial descartável, luvas, óculos de proteção e avental o tempo todo). Rituais funerários tradicionais, especialmente aqueles que requerem o embalsamamento de corpos, devem ser desencorajados ou modificados.
No laboratório
Os vírus de Marburg são patógenos do grupo de risco 4 da Organização Mundial da Saúde, exigindo contenção equivalente ao nível 4 de biossegurança (BSL-4), sendo que os pesquisadores de laboratório devem ser treinados adequadamente nas práticas BSL-4 e usar equipamentos de proteção individual adequados.
Tratamento
Atualmente, não há terapia específica eficaz contra o vírus de Marburg para o tratamento da MVD. O tratamento é principalmente de natureza de suporte e inclui a minimização de procedimentos invasivos, balanceamento de fluidos e eletrólitos para combater a desidratação, administração de anticoagulantes no início da infecção para prevenir ou controlar a coagulação intravascular disseminada, administração de pró-coagulantes no final da infecção para controlar a hemorragia, manutenção dos níveis de oxigênio, controle da dor, e administração de antibióticos ou antifúngicos para tratar infecções secundárias.
Prognóstico
O prognóstico geralmente é ruim. Se o paciente sobreviver, a recuperação pode ser rápida e completa ou prolongada com sequelas, como orquite, hepatite, uveíte, parotidite, descamação ou alopecia. É importante ressaltar que a MARV é conhecida por ser capaz de persistir em alguns sobreviventes e reativar e causar um surto secundário da MVD ou ser transmitida via esperma, causando casos secundários de infecção e doença.
Das 252 pessoas que contraíram Marburg durante o surto de 2004–2005 de um serotipo particularmente virulento em Angola, 227 morreram, para uma taxa de letalidade de 90%. Embora todas as faixas etárias sejam suscetíveis à infecção, as crianças raramente são infectadas. Na epidemia do Congo de 1998–2000, apenas 8% dos casos eram crianças com menos de 5 anos de idade.
Epidemiologia
Abaixo está uma tabela de surtos relativos à doença do vírus de Marburg (MVD) de 1967 a 2023:
| Ano | País | Vírus | Casos humanos | Mortes humanas | Taxa de letalidade | Ref. |
|---|---|---|---|---|---|---|
| 1967 |
|
MARV | 31 | 7 | 23% | |
| 1975 |
|
MARV | 3 | 1 | 33% | |
| 1980 |
|
MARV | 2 | 1 | 50% | |
| 1987 |
|
RAVV | 1 | 1 | 100% | |
| 1988 |
|
MARV | 1 | 1 | 100% | |
| 1990 |
|
MARV | 1 | 0 | 0% | |
| 1998–2000 |
|
MARV & RAVV | 154 | 128 | 83% | |
| 2004–2005 |
|
MARV | 252 | 227 | 90% | |
| 2007 |
|
MARV & RAVV | 4 | 1 | 25% | |
| 2008 |
|
MARV | 2 | 1 | 50% | |
| 2012 |
|
MARV | 18 | 9 | 50% | |
| 2014 |
|
MARV | 1 | 1 | 100% | |
| 2017 |
|
MARV | 3 | 3 | 100% | |
| 2021 |
|
MARV | 1 | 1 | 100% | |
| 2022 |
|
MARV | 3 | 2 | 66.66% | |
| 2023 |
|
MARV | 25 | 11 | 44% |
Surto de 1967
A MVD foi documentada pela primeira vez em 1967, quando 31 pessoas adoeceram nas cidades alemãs de Marburg e Frankfurt am Main, e em Belgrado, Iugoslávia. O surto envolveu 25 infecções primárias por MARV e sete mortes, e seis casos secundários não letais. O surto foi atribuído a macacos Chlorocebus aethiops infectados importados de um local não revelado em Uganda e usados no desenvolvimento de vacinas contra a poliomielite. Os macacos foram recebidos pela Behringwerke, empresa de Marburg fundada pelo primeiro ganhador do Prêmio Nobel de Medicina, Emil Adolf von Behring. A empresa, que na época era propriedade da Hoechst AG, foi originalmente criada para desenvolver soros contra tétano e difteria. Infecções primárias ocorreram na equipe do laboratório da Behringwerke enquanto trabalhavam com tecidos de Chlorocebus aethiops ou culturas de tecidos sem equipamento de proteção individual adequado. Casos secundários envolveram dois médicos, uma enfermeira, um atendente post-mortem e a esposa de um veterinário. Todos os casos secundários tiveram contato direto, geralmente envolvendo sangue, com um caso primário. Ambos os médicos foram infectados por picadas acidentais na pele ao coletar sangue de pacientes. Um relato científico popular desse surto pode ser encontrado no livro The Coming Plague, de Laurie Garrett.
Casos de 1975
Em 1975, um turista australiano foi infectado com MARV na Rodésia (hoje Zimbábue). Ele morreu em um hospital em Joanesburgo, África do Sul. Sua namorada e uma enfermeira assistente foram posteriormente infectadas com MVD, mas sobreviveram.
Casos de 1980
Um caso de infecção por MARV ocorreu em 1980 no Quênia. Um francês, que trabalhava como engenheiro elétrico em uma fábrica de açúcar em Nzoia (perto de Bungoma), na base do Monte Elgon (que contém a caverna Kitum), foi infectado por meios desconhecidos e morreu em 15 de janeiro, logo após ser internado no Hospital de Nairóbi. O médico assistente contraiu MVD, mas sobreviveu. Um relato científico popular desses casos pode ser encontrado no livro The Hot Zone, de Richard Preston (o francês é referido sob o pseudônimo de "Charles Monet", enquanto o médico é identificado sob seu nome verdadeiro, Shem Musoke).
Caso de 1987
Em 1987, um único caso letal de infecção por RAVV ocorreu em um menino dinamarquês de 15 anos, que passava férias em Kisumu, no Quênia. Ele havia visitado a caverna Kitum no Monte Elgon antes de viajar para Mombasa, onde desenvolveu sinais clínicos de infecção. O menino morreu após ser transferido para o Hospital de Nairóbi. Um relato científico popular deste caso pode ser encontrado no livro The Hot Zone, de Richard Preston (o menino é referido sob o pseudônimo de "Peter Cardinal").
Infecção laboratorial de 1988
Em 1988, o pesquisador Nikolai Ustinov infectou-se letalmente com MARV após se picar acidentalmente com uma seringa usada para inoculação de porquinhos-da-índia. O acidente ocorreu na Associação de Produção Científica "Vektor" (hoje Centro Estadual de Pesquisa de Virologia e Biotecnologia "Vektor") em Koltsovo, União Soviética (hoje Rússia). Muito pouca informação está disponível publicamente sobre este caso de MVD, porque os experimentos de Ustinov foram confidenciais. Um relato científico popular desse caso pode ser encontrado no livro Biohazard, de Ken Alibek.
Infecção laboratorial de 1990
Outro acidente de laboratório ocorreu na Associação de Produção Científica "Vektor" (hoje Centro Estadual de Pesquisa em Virologia e Biotecnologia "Vektor") em Koltsovo, União Soviética (hoje Rússia), quando um cientista contraiu MARV por meios desconhecidos.
Surto de 1998–2000
Um grande surto de MVD ocorreu entre garimpeiros ilegais ao redor da mina de Goroumbwa em Durba e Watsa, República Democrática do Congo, de 1998 a 2000, quando a co-circulação de MARV e RAVV causou 154 casos de MVD e 128 mortes. O surto terminou com a inundação da mina.
Surto de 2004–2005
No início de 2005, a Organização Mundial da Saúde (OMS) começou a investigar um surto de febre hemorrágica viral em Angola, centrado na província de Uíge, no nordeste, mas que também afetou muitas outras províncias. O governo angolano teve que pedir ajuda internacional, lembrando que havia apenas cerca de 1 200 médicos em todo o país, com algumas províncias tendo apenas dois. Os profissionais de saúde também reclamaram da falta de equipamentos de proteção individual, como luvas, aventais e máscaras. A Médicos sem Fronteiras (MSF) relatou que, quando sua equipe chegou ao hospital provincial no centro do surto, eles o encontraram funcionando sem água e eletricidade. O rastreamento de contatos foi complicado pelo fato de que as estradas do país e outras infraestruturas foram devastadas após quase três décadas de guerra civil e o campo permaneceu repleto de minas terrestres. O Hospital Américo Boa Vida, na capital angolana de Luanda, montou uma ala especial de isolamento para tratar os infectados do interior. Infelizmente, como a MVD geralmente resulta em morte, algumas pessoas passaram a ver hospitais e profissionais de saúde com desconfiança e trataram os ajudantes com hostilidade. Por exemplo, uma enfermaria de isolamento especialmente equipada no hospital da província de Uíge ficou vazia durante grande parte da epidemia, embora a instalação estivesse no centro do surto. A OMS foi forçada a implementar o que descreveu como uma "estratégia de redução de danos", que consistia na distribuição de desinfetantes para as famílias afetadas que recusaram atendimento hospitalar. Das 252 pessoas que contraíram MVD durante o surto, 227 morreram. Foi o maior surto registrado da doença do vírus de Marburg.
Casos de 2007
Em 2007, quatro mineradores foram infectados com o vírus de Marburg no distrito de Kamwenge, Uganda. O primeiro caso, um homem de 29 anos, tornou-se sintomático em 4 de julho de 2007, e foi internado em um hospital três dias depois, mas acabou por morrer em 13 de julho. O rastreamento de contatos revelou que o homem teve contato próximo prolongado com dois colegas (um homem de 22 anos e um homem de 23 anos), que apresentaram sinais clínicos de infecção antes do início da doença. Ambos os homens foram internados em hospitais em junho e sobreviveram às infecções, comprovadamente devidas ao MARV. Um quarto homem, de 25 anos, desenvolveu sinais clínicos de MVD em setembro e demonstrou estar infectado com RAVV. Ele também sobreviveu à infecção.
Casos de 2008
Em 10 de julho de 2008, o Instituto Nacional de Saúde Pública e Meio Ambiente dos Países Baixos informou que uma neerlandesa de 41 anos, que visitou a caverna Python na floresta de Maramagambo durante suas férias em Uganda, teve MVD devido à infecção por MARV e foi internada em um hospital nos Países Baixos. A mulher morreu em tratamento no Centro Médico da Universidade de Leiden em 11 de julho. O Ministério da Saúde de Uganda fechou a caverna após este caso. Em 9 de janeiro daquele ano, um médico infectologista notificou o Departamento de Saúde Pública e Meio Ambiente do Colorado que uma estadunidense de 44 anos que havia retornado de Uganda havia sido hospitalizada com febre de origem desconhecida. Na época, o teste sorológico foi negativo para febre hemorrágica viral. Ela recebeu alta em 19 de janeiro de 2008. Após a morte da paciente neerlandesa e a descoberta de que a estadunidense havia visitado a Caverna Python, testes adicionais confirmaram que a paciente apresentava anticorpos MARV e RNA.
Surto em Uganda em 2017
Em outubro de 2017, um surto da doença do vírus de Marburg foi detectado no distrito de Kween, leste de Uganda. Todos os três casos iniciais (pertencentes a uma família – dois irmãos e uma irmã) morreram em 3 de novembro. O quarto caso – um profissional de saúde – desenvolveu sintomas em 4 de novembro e foi internado em um hospital. O primeiro caso confirmado viajou para o Quênia antes da morte. Um contato próximo do segundo caso confirmado viajou para Kampala. Foi relatado que várias centenas de pessoas podem ter sido expostas à infecção.
Casos na Guiné em 2021
Em agosto de 2021, dois meses após o fim da epidemia de ébola reemergente na província de Guéckédou, um caso da doença do vírus de Marburg foi confirmado pelas autoridades de saúde por meio de análises laboratoriais. Outro caso potencial da doença em um contato estava aguardando resultados oficiais. Este tinha sido o primeiro caso confirmado de febre hemorrágica de Marburg na África Ocidental. O caso de Marburg também foi identificado em Guéckédou. Durante o surto, um total de um caso confirmado que morreu (CFR = 100%) e 173 contatos foram identificados, incluindo 14 contatos de alto risco com base na exposição. Entre eles, 172 foram acompanhados por um período de 21 dias, dos quais nenhum desenvolveu sintomas. Um contato de alto risco foi perdido durante o acompanhamento. O sequenciamento isolado do paciente guineense mostrou que esse surto foi causado pelo vírus de Marburg, semelhante aos casos em Angola. Uma colônia de morcegos frugívoros egípcios (reservatório hospedeiro do vírus de Marburg) foi encontrada nas proximidades (4,5 km) da vila, onde o surto da doença do vírus de Marburg surgiu em 2021. Dois dos morcegos frugívoros amostrados desta colônia foram PCR positivos para o vírus de Marburg.
Casos na Gana em 2022
Em julho de 2022, a análise preliminar de amostras coletadas de dois pacientes – ambos falecidos – em Gana indicou que os casos eram positivos para o vírus de Marburg. No entanto, por procedimento padrão, as amostras foram enviadas ao Instituto Pasteur de Dakar para confirmação. Em 17 de julho de 2022, os dois casos foram confirmados por Gana, o que levou o país a declarar um surto da doença do vírus de Marburg. Um caso adicional foi identificado, elevando o total para três.
Surto na Guiné Equatorial em 2023
Em fevereiro de 2023, a Guiné Equatorial relatou um surto da doença do vírus de Marburg. Até 28 de fevereiro de 2023, havia um caso confirmado, 24 casos suspeitos e 11 mortes confirmadas devido à doença.
Investigação
Experimentalmente, o vírus recombinante da estomatite vesicular expressando a glicoproteína de MARV foi usado com sucesso em modelos de primatas não humanos como profilaxia pós-exposição. Uma vacina candidata foi eficaz em primatas não humanos. Regimes terapêuticos experimentais baseados na tecnologia antisense mostraram-se promissores, com oligômeros de morfolino fosforodiamidato visando o genoma MARV. Novas terapias de Sarepta e Tekmira também foram usadas com sucesso em humanos e primatas.
Leituras adicionais
Ligações externas
- ViralZone: Vírus de Marburg (em inglês). Consultado em 16 de fevereiro de 2023
- Centros de Controle e Prevenção de Doenças, Controle de Infecção para Febres Hemorrágicas Virais no Ambiente Africano de Cuidados de Saúde (em inglês). Consultado em 16 de fevereiro de 2023
- Centro de Controle e Prevenção de Doenças, Febre Hemorrágica de Marburg (em inglês). Consultado em 16 de fevereiro de 2023
- Centro de Controle e Prevenção de Doenças, Casos conhecidos e surtos de febre hemorrágica de Marburg (em inglês). Consultado em 16 de fevereiro de 2023
- Ebola e febre hemorrágica de Marburg – Ficha informativa do Centro Europeu de Prevenção e Controlo das Doenças (em inglês). Consultado em 16 de fevereiro de 2023
- Organização Mundial da Saúde, Febre Hemorrágica de Marburg (em inglês). Consultado em 16 de fevereiro de 2023
- Cruz Vermelha PDF (em inglês). Consultado em 16 de fevereiro de 2023
- Virus Banco de dados de patógenos e recurso de análise: Filoviridae (em inglês). Consultado em 16 de fevereiro de 2023
| Identificadores |
|---|
| |||||||||||||||||||||||||||||||||||||