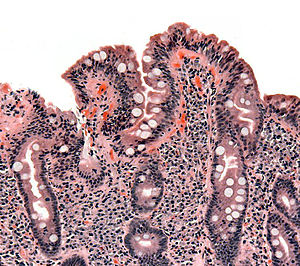
Doença celíaca
Doença celíaca é uma doença autoimune crónica do intestino delgado causada por uma reação ao glúten em pessoas com predisposição genética. Os sintomas clássicos incluem problemas gastrointestinais como diarreia crónica, distensão abdominal, má-absorção intestinal e perda de apetite. Em crianças, pode ocorrer atraso no crescimento que geralmente se inicia entre os seis meses e dois anos de idade. Os sintomas não clássicos são mais comuns, especialmente em pessoas com mais de dois anos. A pessoa pode não manifestar sintomas gastrointestinais ou manifestar apenas sintomas gastrointestinais ligeiros, podem ocorrer sintomas em qualquer parte do corpo, ou não haver sintomas visíveis de todo. Embora a doença celíaca seja geralmente diagnosticada durante a infância, pode aparecer em qualquer idade. A doença está associada a outras doenças autoimunes, como diabetes mellitus tipo 1 e tiroidite, entre outras.
A doença celíaca é causada por uma reação do organismo ao glúten, um conjunto de proteínas presentes no trigo e em outros cereais como a cevada ou centeio. A aveia em quantidades moderadas é geralmente tolerada, dependendo da variedade e desde que não esteja contaminada com outros cereais com glúten. Ao ser exposto ao glúten, o sistema imunitário desencadeia uma resposta anormal, produzindo uma série de anticorpos que podem afetar diversos órgãos. No intestino delgado, esta resposta imunitária provoca uma reação inflamatória que faz diminuir as vilosidades intestinais. Isto afeta a absorção de nutrientes pelo intestino, o que em muitos casos causa anemia.
O diagnóstico é geralmente feito com análises aos anticorpos do sangue e uma biópsia do intestino, podendo ser apoiado por exames genéticos. No entanto, o diagnóstico nem sempre é conclusivo. Em muitos celíacos, o exame aos anticorpos é negativo e muitos indivíduos apresentam apenas ligeiras alterações intestinais com vilosidades normais. Em alguns casos, o diagnóstico pode levar anos para ser confirmado, mesmo que as pessoas sejam examinadas e manifestem sintomas pronunciados. Com o avanço das técnicas de rastreio, é cada vez mais comum o diagnóstico de doença celíaca entre pessoas assintomáticas. No entanto, não há ainda evidências conclusivas que apoiem a eficácia do rastreio sistemático. Embora a doença seja causada por uma intolerância permanente às proteínas do trigo, não se trata de uma forma de alergia ao trigo.
O único tratamento eficaz conhecido é seguir uma dieta sem glúten durante toda a vida. A ausência de glúten permite a reparação das mucosas do intestino, alivia os sintomas e diminui o risco de complicações na maioria das pessoas. Quando a doença não é tratada, pode levar ao aparecimento de cancros como o linfoma intestinal e a um ligeiro aumento do risco de morte prematura. A frequência da doença varia entre as diferentes regiões do mundo, desde 1 em cada 300 pessoas até 1 em cada 40 pessoas. A média é de entre 1 em cada 100-170 pessoas. Nos países desenvolvidos, estima-se que 80% dos casos não cheguem a ser diagnosticados, geralmente devido à ausência de sintomas gastrointestinais e ao pouco conhecimento da doença entre a população. A doença celíaca é ligeiramente mais comum entre mulheres do que em homens. O termo "celíaco" tem origem no grego κοιλιακός (koiliakós, "abdominal"), tendo sido introduzido na linguagem contemporânea durante o século XIX numa tradução do que é geralmente considerada a primeira descrição da doença por Areteu da Capadócia.
Sinais e sintomas
A doença celíaca grave manifesta-se através de sintomas característicos, como fezes claras, fétidas, acompanhadas de gordura e flutuantes (esteatorreia), perda de peso ou incapacidade de ganhar peso (no caso de crianças). As pessoas com doença moderada podem manifestar sintomas muito mais subtis e em outros órgãos para além do próprio intestino. É também possível ter doença celíaca sem manifestar quaisquer sintomas. Muitos adultos com doença leve apenas apresentam fadiga ou anemia.
Gastrointestinais
A diarreia característica da doença celíaca é clara, volumosa e anormalmente fétida. São também comuns cãibras e dores abdominais, sensação de barriga inchada com distensão abdominal (que se pensa ser devida à fermentação de gases intestinais) e úlceras na boca. À medida que aumentam as lesões no intestino é possível que se desenvolva intolerância à lactose de grau variável. Em muitos casos, os sintomas são inicialmente atribuídos à síndrome do intestino irritável (SII), só sendo mais tarde confirmada a doença celíaca. Uma pequena percentagem dos casos de pessoas com sintomas de SII tem doença celíaca, sendo recomendado o rastreio para quem manifeste sintomas de SII.
A doença celíaca aumenta o risco de adenocarcinoma e linfoma do intestino delgado (linfoma de células T associado a enteropatia (EATL) ou outros linfomas não Hodgkin). Este risco é também acrescido em parentes em primeiro grau e ainda não é claro se após a adesão a uma dieta isenta de glúten este risco volta ou não aos valores normais. Caso a doença não seja tratada após um longo intervalo de tempo é possível que surjam outras complicações, como jejunite ulcerativa (formação de úlceras no intestino delgado) e estreitamento e obstrução do intestino devido à cicatrização).
Relacionados com a má absorção
As alterações no intestino diminuem a sua capacidade de absorver nutrientes, sais minerais e as vitaminas lipossolúveis A, D, E e K.
- A incapacidade em absorver hidratos de carbono e gorduras pode provocar perda de peso (ou, em crianças, atraso no desenvolvimento fisiológico), fadiga ou falta de energia.
- A anemia pode desenvolver-se de várias formas: a má absorção de ferro pode provocar anemia por deficiência de ferro, enquanto que a má absorção de ácido fólico e vitamina B12 pode provocar anemia megaloblástica.
- A má absorção de cálcio e vitamina D (e o hiperparatiroidismo compensatório secundário) podem provocar osteopenia (diminuição da quantidade de mineral no osso) ou osteoporose (enfraquecimento do osso e risco de fraturação).
- A má absorção de selénio, em conjugação com o baixo teor de selénio em muitos dos alimentos isentos de glúten, agrava o risco de hiposselenemia,
- Estão também associadas à doença deficiências em cobre e zinco.
- Uma pequena percentagem dos celíacos apresenta coagulação anormal devido à deficiência de vitamina K, o que agrava o risco de hemorragias.
- A doença celíaca está também associada ao crescimento excessivo das bactérias do intestino delgado, o que pode agravar ainda mais a má absorção ou causar má absorção mesmo com o tratamento.
Outros sintomas
A doença celíaca tem sido associada a diversas condições. Em muitos casos, não é ainda claro se a causa destas condições é a própria doença induzida pelo glúten ou se têm todas origem numa predisposição comum.
- A deficiência de imunoglobulina A ocorre em 2,3% das pessoas com doença celíaca e, por sua vez, esta condição agrava em dez vezes o risco de vir a ter doença celíaca. Esta condição também agrava o risco de infeções e de doenças autoimunes.
- Dermatite herpetiforme, uma condição cutânea comichosa que tem sido associada à enzima transglutaminase presente na pele. Manifesta-se por alterações no intestino delgado idênticas às da doença celíaca e pode responder à remoção de glúten, mesmo na inexistência de sintomas gastrointestinais.
- Durante a infância, pode ocorrer atraso no crescimento e/ou na puberdade, mesmo perante a inexistência de sintomas intestinais óbvios ou desnutrição grave. O diagnóstico de atraso no desenvolvimento muitas vezes inclui o rastreio de doença celíaca.
- Podem ocorrer complicações na gravidez devido à doença celíaca, entre as quais aborto espontâneo, atraso no desenvolvimento do feto, parto pré-termo ou baixo peso à nascença.
- Hipoesplenismo, ou baço pequeno e pouco ativo, condição que ocorre em cerca de um terço dos casos e pode predispor a pessoa para uma infeção, dado o papel do baço na proteção contra bactérias.
- Testes de função hepática fora do normal.
A doença celíaca está ainda associada a diversas outras condições médicas, muitas das quais são doenças autoimunes: diabetes mellitus tipo 1, hipotiroidismo, cirrose biliar primária e colite microscópica.
Uma associação mais controversa está relacionada com um grupo de doenças nas quais são detetados anticorpos anti-gliadina, mas não é possível demonstrar qualquer doença do intestino delgado. Por vezes estas condições melhoram após remover o glúten da dieta. Entre elas estão a ataxia cerebelar, neuropatia periférica, esquizofrenia e autismo.
Causas
A doença celíaca é causada por uma reação à gliadina, uma prolamina (proteína do glúten) presente no trigo, e a proteínas semelhantes presentes na tribo das Triticeae (que inclui outros cereais comuns como a cevada e o centeio).
Outros cereais
Algumas subespécies de trigo, como a espelta, e algumas espécies relacionadas, como a cevada, o centeio ou o triticale, também induzem sintomas da doença celíaca. Uma pequena minoria das pessoas com a doença também reagem à aveia. É provável que a aveia induza sintomas devido à contaminação cruzada com outros cereais nas zonas de cultivo ou nos canais de distribuição, pelo que o seu consumo geralmente não é recomendado a celíacos. No entanto, algumas empresas garantem a pureza da aveia, pelo que pode continuar a ser consumida por este meio.
O consumo de outros cereais, como o milho, painço, sorgo, teff, arroz ou arroz selvagem, é seguro para celíacos, assim como não cereais como o amaranto, quinoa ou o trigo mourisco. Outros alimentos não cereais, como as batatas ou as bananas, não contêm glúten e não desencadeiam sintomas.
Modificadores de risco
Existem várias teorias sobre o que determina se um indivíduo geneticamente predisposto desenvolve ou não doença celíaca. Entre as principais teorias estão a infeção por rotavírus ou adenovírus intestinal humano. Alguma investigação tem sugerido que fumar oferece alguma proteção contra o aparecimento da doença na fase adulta.
As pessoas expostas ao trigo, cevada ou centeio antes de terem a flora intestinal completamente desenvolvida (nos três meses posteriores ao nascimento) apresentam um risco cinco vezes superior de desenvolver doença celíaca em comparação com as pessoas expostas apenas quatro a seis meses após o nascimento. Os que são expostos após os seis meses apresentam um risco ligeiramente superior em comparação com aqueles expostos entre os quatro e seis meses. A introdução precoce de cereais na vida das pessoas oferece proteção contra as alergias a cereais. A amamentação pode também oferecer proteção em relação ao desenvolvimento da doença. Amamentar durante a introdução do glúten na dieta e aumentar a duração do período de amamentação estão associados a um menor risco de vir a desenvolver doença celíaca, embora ainda não seja claro se os benefícios são permanentes ou se apenas atrasa os sintomas. Entre outros fatores que podem desencadear sintomas estão as cirurgias, a gravidez, infeções e stresse emocional.
Diagnóstico
Existem diversos exames que podem ser usados como meio de diagnóstico, sendo a realização determinada em função da intensidade dos sintomas. No entanto, todos os exames perdem utilidade caso a pessoa já se encontre a fazer uma dieta isenta de glúten. Após a remoção do glúten da dieta, as lesões no intestino delgado começam a curar no prazo de poucas semanas e a quantidade de anticorpos diminui no prazo de alguns meses. Para o correto diagnóstico destas pessoas, pode ser necessária a ingestão de alguns produtos com glúten numa das refeições diárias e ao longo de seis semanas.
A combinação das observações numa regra de predição para orientar o uso de uma biópsia endoscópica apresenta uma sensibilidade de 100% (identificaria todos os casos) numa população de indivíduos com elevado índice de suspeita para a doença celíaca, com especificidade de 61% (39% de falsos positivos). A regra de predição recomenda que as pessoas com sintomas de elevado risco ou serologia positiva se devem submeter a uma biópsia endoscópica da segunda parte do duodeno. Os sintomas de elevado risco são a perda de peso, anemia (hemoglobina inferior a 120 g/l em mulheres ou 130 g/l em homens) ou diarreia (mais de três fezes líquidas por dia).
Exames sanguíneos
Os exames sanguíneos serológicos são a primeira linha de investigação para confirmar um diagnóstico de doença celíaca. Os anticorpos endomisiais do tipo imunoglobulina A (IgA) são capazes de detetar a doença com uma sensibilidade e especificidade de 90% e 99%, respetivamente. A serologia de anticorpos anti-tTG foi inicialmente reportada como tendo maior sensibilidade (99%) e especificidade (90%). No entanto, atualmente pensa-se que tenha características semelhantes aos anticorpos anti-endomisiais. Os exames anti-tTG atuais têm por base uma proteína recombinante humana como antígeno. O exame tTG é geralmente o primeiro a ser realizado por ser o mais simples de executar. Um resultado ambíguo de tTG é geralmente seguido por um exame de anticorpos endomisiais.
Devido às profundas implicações que um diagnóstico de doença celíaca representa, as orientações profissionais recomendam que um exame sanguíneo positivo seja mesmo assim seguido por uma esofagogastroduodenoscopia/endoscopia e biópsia. Caso continue a existir suspeita clínica após um exame serológico negativo, pode também ser feita uma recomendação de endoscopia e biópsia ao duodeno, devido à taxa de 1% de falsos negativos que os exames apresentam. Por este motivo, a biópsia continua a ser considerada o padrão-ouro no diagnóstico de doença celíaca. As orientações recomendam também que seja realizado em paralelo o exame da quantidade de IgA no soro, já que os celíacos com insuficiência de IgA podem ser incapazes de produzir os anticorpos em que os outros exames se baseiam, dando origem a falsos negativos.
No passado eram medidos três outros anticorpos: os anticorpos anti-reticulina (ARA), anti-gliadina e anti-endomísio. No entanto, o exame aos anticorpos ARA não é suficientemente preciso para diagnósticos de rotina. A serologia pode ser pouco fidedigna em crianças mais novas, embora o exame aos anticorpos anti-gliadina seja ligeiramente mais fidedigno do que outros exames em crianças com idade inferior a cinco anos.
Os exames serológicos usam a técnica de imunofluorescência indireta (reticulina, gliadina e endomísio) ou o método ELISA (gliadina ou tTG). Os exames para a presença de anticorpos e os exames para a presença de antígeno leucocitário humano (HLA) têm precisão equivalente; no entanto, atualmente não é recomendada a utilização de HLA no diagnóstico de doença celíaca.
Endoscopia

Geralmente é realizada uma biópsia do duodeno ou do jejuno. São recolhidas entre quatro e oito amostras de tecido, já que as áreas podem não ser afetadas por igual e se a amostra for recolhida a partir de uma área saudável pode dar origem a falsos negativos.
Na maior parte das pessoas com doença celíaca, o intestino delgado apresenta-se normal durante uma endoscopia. No entanto, existem cinco observações endoscópicas que sugerem doença celíaca: pregas mucosas serrilhadas, padrão em mosaico da mucosa (semelhante ao padrão de lama seca), proeminência dos vasos sanguíneos da submucosa e padrão nodular da mucosa.
Até à década de 1970, as biópsias eram realizadas com cápsulas de metal ligadas a um dispositivo de sucção. A cápsula era engolida e transitava até ao intestino delgado. Após ser confirmada a sua posição através de raio X, era aplicada sucção para recolher parte da parede intestinal para o interior da cápsula. Este método foi em grande parte substituído pela endoscopia de fibra ótica, com maior sensibilidade e menor taxa de erro.
Patologia
As alterações patológicas clássicas da doença celíaca no intestino delgado são categorizadas de acordo com a Classificação de Marsh:
- Estádio 0: mucosa normal
- Estádio 1: infiltração linfocitária intraepitelial superior a 20 por cada 100 enterócitos
- Estádio 2: proliferação das criptas intestinais
- Estádio 3: atrofia parcial ou total das vilosidades intestinais e hipertrofia das criptas
- Estádio 4: hipoplasia da constituição do intestino delgado
A classificação de Marsh, introduzida em 1992, foi posteriormente modificada em 1999 para seis estádios, tendo o estádio 3 sido dividido em três sub-estágios. Os estudos posteriores demonstraram que este sistema nem sempre era fidedigno e que as alterações observadas na doença celíaca podiam ser descritas em um de três estágios — A, B1 e B2 — em que A representa a infiltração linfocitária com aparência das vilosidades normal e em que B1 e B2 descrevem a atrofia parcial ou total das vilosidades.
Estas alterações geralmente melhoram ou são revertidas após a remoção do glúten da dieta. No entanto, a maior parte das orientações não recomenda repetir a biópsia a não ser que não se verifique a melhoria dos sintomas com a dieta. Em alguns casos pode ser prescrita a ingestão temporária de glúten, seguida por biópsia, para confirmar ou refutar o diagnóstico. Uma biópsia e serologia normais após este teste podem indicar que o diagnóstico inicial foi incorreto.
Outros exames de diagnóstico
Durante o diagnóstico podem ser realizados outros exames para identificar complicações, como a deficiência de ferro (através de hemograma), deficiência de ácido fólico ou vitamina B12 e hipocalcemia (diminuição do nível de cálcio, geralmente devido à diminuição de vitamina D). Podem também ser realizados exames à função da tiroide juntamente com os exames sanguíneos de modo a identificar hipotiroidismo, o qual é mais comum entre celíacos. A osteopenia e a osteoporose (diminuição da densidade mineral dos ossos) estão muitas vezes presentes em pessoas com a doença, pelo que durante o diagnóstico podem ser realizados exames para medição da densidade óssea para avaliar o risco de fraturas e a necessidade de medicação para proteção óssea, como a varredura por absorciometria bifotónica de raio X (DXA).
Fisiopatologia
Praticamente todas as pessoas com doença celíaca ou têm o alelo HLA-DQ2 ou, menos frequentemente, o alelo HLA-DQ8. No entanto, cerca de 20-30% das pessoas sem a doença também herdaram um destes alelos. Isto sugere que são necessários outros fatores para que a doença se desenvolva; isto é, que o alelo HLA é condição necessária, mas não suficiente, para desenvolver doença celíaca. Além disso, cerca de 5% das pessoas que desenvolvem a doença não apresenta os alelos HLA-DQ2 ou HLA-DQ8.
Genética
A vasta maioria das pessoas com doença celíaca têm um de dois tipos da proteína HLA-DQ. Existem sete variantes HLA-DQ (DQ2 e DQ4 a DQ9). Mais de 95% das pessoas com doença celíaca têm a isoforma DQ2 ou DQ8, a qual é herdade entre a família. Estes genes aumentam o risco de doença celíaca porque os seus recetores ligam-se aos peptídeos de gliadina mais firmemente do que outras formas do recetor apresentador de antígeno. Assim, estas formas do recetor têm maior probabilidade de ativar os linfócitos T e dar início ao processo autoimune.
A maior parte dos celíacos apresenta um haplotipo HLA-DQ2 de dois genes designado haplotipo DQ2.5. Este haplotipo é composto por dois alelos génicos, DQA1*0501 e DQB1*0201, os quais codificam as duas subunidades, DQ α5 e DQ β2. Na maior parte das pessoas, esta isoforma DQ2.5 é codificada por um de dois cromossomas 6 herdado dos pais (DQ2.5cis). A maioria dos celíacos herda apenas uma cópia deste haplotipo DQ2.5, enquanto os restantes herdam-no de ambos os pais. Estes últimos apresentam um risco particularmente elevado de doença celíaca e são mais suscetíveis a complicações graves.
Algumas pessoas herdam o DQ2.5 de um dos pais e uma parte adicional do haplotipo do outro progenitor, o que aumenta o risco. Ainda que de forma menos comum, algumas pessoas herdam o alelo DQA1*05 de um dos pais e o DQB1*02 do outro (DQ2.5trans) (situação que se denomina "associação trans-haplotipo"). Estas pessoas apresentam risco idêntico de contrair a doença em relação àquelas com um único cromossoma 6 DQ2.5, embora neste caso a doença não tenha tendência a ser familiar. Entre os 6% de celíacos na Europa que não têm o DQ2.5 (cis ou trans) ou o DQ8 (codificado pelo haplotipo DQA1*03:DQB1*0302), 4% têm a isoforma DQ2.2 e os restantes 2% não têm nem o DQ2 nem o DQ8.
A frequência destes genes varia consoante a região. O DQ2.5 é mais frequente entre pessoas do norte e oeste da Europa, em particular no País Basco e na Irlanda, e em partes de África, estando ainda associada à doença na Índia, mas não se encontra em grande parte da costa do Pacífico. O DQ8 está mais distribuído do que o DQ2.5 e é especialmente comum na América Central e do Sul. Cerca de 90% dos indivíduos de algumas populações ameríndias apresentam o DQ8, pelo que podem apresentar o fenótipo celíaco.
Têm também sido sucessivamente reportados outros fatores genéticos na doença celíaca. No entanto, a aceitação do seu envolvimento na doença varia conforme a região. Só o loci HLA-DQ demonstra estar envolvido de forma consistente na população mundial. Muitos dos loci detetados estão associados a outras doenças autoimunes. Um locus, o gene LPP (lipoma-preferred partner), está envolvido na aderência de matrizes extracelulares à superfície da célula. Uma variante menor (SNP = rs1464510) aumenta o risco da doença em cerca de 30%.
Esta prevalência de genótipos de doença celíaca na população contemporânea ainda não é completamente compreendida. Dadas as características da doença e a sua aparente forte hereditariedade, seria de esperar que os genótipos sofressem seleção negativa e estivessem ausentes em sociedades onde a agricultura fosse praticada há mais tempo; compare-se, por exemplo, com a intolerância à lactose, uma condição semelhante que sofreu seleção negativa de tal forma que a sua prevalência diminuiu de aproximadamente 100% nas populações da antiguidade para menos de 5% em alguns países europeus. No entanto, não aparenta ser o caso; pelo contrário, existem evidências de seleção positiva nos genótipos de doença celíaca. Suspeita-se que alguns deles possam ter sido benéficos ao proporcionar proteção contra infeções bacterianas.
Prolaminas
A maioria das proteínas alimentares responsável pela reação imunitária na doença celíaca são as prolaminas. As prolaminas são proteínas de armazenamento ricas em prolina que se dissolvem em álcoois e são resistente às proteases e peptidases do intestino. As prolaminas encontram-se em cereais, tendo cada tipo de cereal prolaminas diferentes, mas relacionadas entre si: trigo (gliadina), cevada (hordeína), centeio (secalina), milho (zeína) e na aveia (avenina). Uma região da α-gliadina estimula as células membranares do intestino para permitir a passagem de moléculas de grande dimensão pelo selante entre as células. A interferência das uniões herméticas permite aos peptídeos maiores do que três aminoácidos entrar na circulação.
A abertura da membrana permite que os peptídeos da gliadina estimulem dois níveis de resposta imunitária, a resposta imunitária inata e a resposta adquirida. Um peptídeo da α-gliadina resistente à protease contém uma região que estimula linfócitos, o que provoca a libertação de interleucina 15. Esta resposta inata à gliadina por sua vez provoca sinalização no sistema imunitário que atrai células inflamatórias e aumenta a libertação de químicos inflamatórios. A resposta adquirida à gliadina mais forte e mais comum é dirigida a um fragmento α2-gliadina com 33 aminoácidos de comprimento.
Esta resposta ocorre em maior parte dos celíacos que têm a isoforma DQ2. Este peptídeo, quando modificado pela transglutaminase intestinal, apresenta uma elevada densidade de epítopos de linfócitos T sobrepostos, o que aumenta a probabilidade de que a isoforma DQ2 se ligue e se mantenha ligada ao peptídeo quando reconhecida pelos linfócitos T. A gliadina do trigo é o membro melhor compreendido desta família, embora existam outras prolaminas capazes de contribuir para a doença celíaca.
Transglutaminase tecidular
Na maioria dos casos da doença, observa-se a presença de anticorpos anti-transglutaminase para a enzima transglutaminase tecidular (tTG). A transglutaminase tecidular modifica os peptídeos de glúten numa forma capaz de estimular o sistema imunitário de forma mais eficaz. Estes peptídeos são modificados pela tTG de duas formas: desaminação ou transaminação.
A desaminação é a reação pela qual se forma um resíduo de glutamato através da clivagem do aminogrupo épsilon de uma cadeia de glutamina. A transaminação, que ocorre com uma frequência três vezes superior, corresponde à ligação cruzada de um resíduo de glutamina com um resíduo de lisina da tTG, numa reação que á catalisada pela transglutaminase. A ligação cruzada pode ocorrer tanto dentro como fora do sítio ativo da enzima. Neste último caso, é produzido um complexo ligado de forma covalente e permanente entre a gliadina e a tTG. Isto leva à formação de novos epítopos, os quais se acredita desencadearem a resposta imunitária primária mediante a qual se desenvolvem os autoanticorpos contra a iTG.
As biópsias de pessoas suspeitas da doença revelaram que os depósitos de autoanticorpos em celíacos sub-clínicos são detetados antes da doença entrar em fase clínica. Estes depósitos também se encontram em pessoas com outras doenças autoimunes, anemia ou fenómenos de má absorção, a taxas muito superiores à população normal. Acredita-se que os componentes endomísios dos anticorpos (EMA) para a tTG sejam destinados à transglutaminase na superfície celular, pelo que estes anticorpos são ainda usados para confirmar um diagnóstico de doença celíaca. No entanto, um estudo de 2006 demonstrou que os celíacos sem EMA tendem a ser homens mais idosos com sintomas abdominais mais graves e menor frequência de sintomas atípicos, incluindo doença autoimune. O mesmo estudo não encontrou relação entre os depósitos de anticorpos anti-tTG e a gravidade da destruição da vilosidades do intestino. Estas descobertas, a par de outras mais recentes que demonstram que a gliadina tem um componente de resposta inata, sugerem que a gliadina possa ter maior responsabilidade nas manifestações primárias da doença celíaca, enquanto que a tTG é um maior fator nos efeitos secundários, como as respostas alérgicas e doenças autoimunes secundárias. Numa grande percentagem de pessoas com doença celíaca, os anticorpos anti-tTG também reconhecem uma proteína de um rotavírus denominada VP7. Estes anticorpos estimulam a proliferação de monócitos e a infeção por rotavírus pode explicar alguns dos estágios iniciais da proliferação de glóbulos brancos. De facto, os primeiros estudos de lesões por rotavírus no intestino demonstram que estes provocam atrofia das vilosidades.
Atrofia das vilosidades e má absorção
O processo inflamatório, mediado pelos linfócitos T, leva à destruição da estrutura e função da mucosa que reveste o intestino delgado. Este processo causa má-absorção intestinal, uma vez que debilita a capacidade do corpo em absorver nutrientes, sais minerais e as vitaminas lipossolúveis A, D, E e K a partir dos alimentos. A diminuição da superfície do intestino e a diminuição da produção de lactase podem também causar intolerância à lactose, embora desapareça quando a condição é tratada.
Têm vindo a ser propostas causas alternativas para estas lesões no tecido que envolvem a libertação de interleucina 15 e a ativação do sistema imune inato por um peptídeo de glúten mais curto (p31–43/49). Este processo desencadearia a morte dos enterócitos pelos linfócitos no epitélio. A atrofia das vilosidades observada nas biópsias pode também ser devida a causas sem relação com a doença, como esprú tropical, giardiose ou exposição a radiação. Embora um resultado serológico positivo e a confirmação por biópsia sejam sugestivos de doença celíaca, na ausência de resposta à dieta pode ser necessário considerar estes diagnósticos alternativos.
Rastreio
Devido à sua elevada sensibilidade, a serologia tem vindo a ser proposta para medida de rastreio, uma vez que a presença de anticorpos detetaria casos não diagnosticados de doença celíaca e preveniria complicações nessas pessoas. No entanto, existe um debate considerável sobre os benefícios do rastreio. Alguns estudos sugerem que a deteção precoce diminuiria o risco de osteoporose e anemia. Por outro lado, um estudo coorte sugeriu que a doença celíaca não diagnosticada apresentava alguns benefícios ao diminuir o risco de doenças cardiovasculares (menos sobrepeso, diminuição do colesterol). Há poucas evidências de que os casos detetados por rastreio beneficiariam de um diagnóstico em termos de morbidade e mortalidade, pelo que atualmente não se acredita que o rastreio de toda a população possa ter benefícios.
No Reino Unido recomenda-se o rastreio de doença celíaca em pessoas a quem foi recentemente diagnosticada síndrome da fadiga crónica, e síndrome do intestino irritável, assim como a diabéticos do tipo 1, em particular daqueles com pouco ganho de peso ou perda de peso inexplicável. O rastreio também é recomendado no caso de tiroidite autoimune, dermatite herpetiforme e nos parentes em primeiro grau de pessoas com doença celíaca confirmada.
Tratamento
Dieta isenta de glúten
Atualmente, o único tratamento eficaz é uma dieta isenta de glúten durante toda a vida. Não existem medicamentos capazes de impedir as lesões ou impedir que o corpo ataque o intestino na presença de glúten. A adesão rigorosa à dieta permite que os intestinos se curem naturalmente, o que na maior parte dos casos leva ao desaparecimento dos sintomas e, se a dieta for iniciada suficientemente cedo, à eliminação do risco acrescido de osteoporose, cancro do cólon e, nalguns casos, da esterilidade.
Geralmente é necessário o acompanhamento de um nutricionista para assegurar que a pessoa tem conhecimento dos alimentos que contêm glúten, daqueles que é seguro ingerir e como conseguir uma dieta equilibrada apesar das limitações. Os produtos sem glúten são geralmente mais caros e difíceis de encontrar do que os produtos normais. Em vários países, os produtos isentos de glúten podem ser receitados e o valor reembolsado através de seguros de saúde. Uma vez que grande parte dos alimentos prontos a comer contêm vestígios de glúten, alguns celíacos consideram que é essencial cozinhar as próprias refeições.
O termo "isento de glúten" encontrado nas embalagens é geralmente usado para indicar uma quantidade alegadamente inócua de glúten, e não a ausência completa. No entanto, a quantidade exata em que o glúten é inócuo é controversa e incerta. Uma revisão sistemática recente concluiu que é improvável que o consumo de menos de 10 mg de glúten por dia possa causar anormalidades histológicas, embora também saliente que ainda tenham sido feitos poucos estudos fidedignos. A regulamentação do rótulo "isento de glúten" varia. Na União Europeia, a Comissão publicou uma diretiva em 2009 que limita o uso do rótulo "isento de glúten" a produtos alimentares com menos de 20 mg/kg de glúten, e o uso do rótulo "teor muito baixo de glúten" a produtos com menos de 100 mg/kg. Nos Estados Unidos, a Food and Drug Administration publicou regulamentação em 2013 que limitava o uso do rótulo "isento de glúten" a produtos com menos de 20 ppm de glúten. O atual padrão internacional Codex Alimentarius permite quantidades até 20 ppm de glúten nos alimentos designados "isentos de glúten".
Mesmo após a adesão a uma dieta rigorosa, a qualidade de vida dos celíacos pode ser menor. Diversos estudos nos Estados Unidos revelaram que a qualidade de vida se torna comparável à generalidade da população após algum tempo na dieta, enquanto que diversos estudos na Europa mostraram que a qualidade de vida se mantém inferior, embora os questionários não sejam idênticos. Os homens tendem a reportar mais melhorias do que as mulheres. Algumas pessoas apresentam sintomas digestivos persistentes ou dermatite herpetiforme, úlceras na boca, osteoporose e respetivas fraturas. Podem ainda manifestar-se sintomas sugestivos de síndrome do intestino irritável e verificar-se um aumento da prevalência de ansiedade, fadiga, dispepsia e dores musculares.
Doença refratária
Numa pequena minoria das pessoas verifica-se doença refratária, o que significa que não melhoram mesmo após uma dieta isenta de glúten. Isto pode dever-se ao facto da doença estar há tanto tempo presente que os intestinos já não são capazes de se regenerar naturalmente, ou pela pessoa não estar a seguir a dieta de forma adequada ou porque a pessoa está a consumir inadvertidamente alimentos contaminados com glúten. Após exclusão de outras causas, nesta situação pode ser considerado o uso de esteroides ou imunossupressores.
Epidemiologia
A doença celíaca afeta em todo o mundo entre 1 em cada 100 e 1 em cada 170 pessoas. No entanto, entre as várias regiões a prevalência varia entre 1 em cada 300 e 1 em cada 40 pessoas. Em vários estudos, a percentagem de pessoas com diagnóstico clínico da doença varia entre 0,05 e 0,27. No entanto, os estudos populacionais de partes da Europa, América do Sul, Australásia e Estados Unidos indicam que a percentagem de pessoas com a doença possa ser entre 0,33-1,06% em crianças e entre 0,18-1,2% em adultos. Entre as pessoas que se apresentam nos cuidados de saúde primários com queixas gastrointestinais, a taxa de diagnósticos de doença celíaca é de cerca de 3%. No passado, pensava-se que a doença celíaca era rara, com prevalência de apenas 0,02%. É possível que o recente aumento no número de casos registados se deva aos avanços nas práticas de diagnóstico. Nos Estados Unidos e na Europa, a prevalência da doença é de 0,75% em grupos fora de risco, o que aumenta para 1,8% em pessoas com sintomas, 2,6% em parentes em segundo grau (avós, tios, etc.) de pessoas com a doença e 4,5% em parentes em primeiro grau (filhos, pais).
As pessoas de ascendência africana, japonesa e chinesa raramente são diagnosticadas, o que é um reflexo da muito menor prevalência de fatores de risco genéticos nestas populações. As pessoas de ascendência indiana e caucasiana apresentam risco idêntico. Os estudos populacionais também indicam que grande parte dos celíacos não chega a ser diagnosticada. Isto deve-se, em parte, ao facto de muitos profissionais de saúde não estarem familiarizados com a condição e ao facto da doença poder ser assintomática. A doença é ligeiramente mais prevalente em mulheres do que em homens. Entre as populações com risco acrescido de ocorrência da doença, em que a taxa de prevalência varia entre 5 e 10%, estão as pessoas com síndrome de Down e de Turner, diabetes tipo 1 e doenças autoimunes da tiroide, incluindo hipertiroidismo e hipotiroidismo.
Sociedade e cultura
Igreja cristã e eucaristia

Diversas denominações cristãs celebram a Eucaristia, na qual é abençoada e ingerida uma hóstia ou um pedaço de pão feitos a partir de trigo. A farinha de trigo contém entre 10 e 13% de glúten, pelo que cada hóstia pode conter mais de 50 mg de glúten, quantidade que é prejudicial à saúde de várias pessoas com doença celíaca, em particular se for consumida diariamente. Muitas igrejas oferecem alternativas sem glúten, geralmente uma bolacha à base de arroz ou pão sem glúten. No entanto, algumas igrejas oferecem apenas hóstias com teor reduzido de glúten, já que as que são completamente isentas de glúten não são consideradas pão de trigo, sendo portanto inapropriadas.
Posição da igreja católica romana
A doutrina católica romana afirma que para uma Eucaristia ser válida, o pão usado na missa deve obrigatoriamente ser feito a partir de trigo. Em 2002, a Congregação para a Doutrina da Fé aprovou hóstias com baixo teor de glúten para serem usadas em Itália. Embora não fossem inteiramente isentas de glúten, foram também aprovadas pela Associação de Celíacos Italiana. Alguns celíacos católicos têm vindo a pedir permissão para o uso de hóstias feitas a partir de arroz. No entanto, estas petições têm sido sempre recusadas. Em janeiro de 2004 passaram a estar disponíveis hóstias com um teor extremamente reduzido de glúten nos Estados Unidos, Itália e Austrália.
Para os padres a questão é mais complexa. Enquanto celebrantes, exige-se que recebam o corpo de Cristo nas duas espécies. Em 2003, a Congregação para a Doutrina da Fé afirmou que "dada a centralidade da celebração da Eucaristia na vida de um padre, deve-se ponderar cuidadosamente antes de admitir à Santa Ordem candidatos que não sejam capazes de ingerir glúten ou álcool sem colocar em risco a sua saúde."
Pessach
O festival judaico do Pessach pode ser problemático para celíacos devido à obrigação de consumir matzá, pão ázimo feito de forma estritamente controlada a partir de trigo, cevada, espelta, aveia ou centeio. Isto exclui diversos outros cereais normalmente usados como substitutos por pessoas com sensibilidade ao glúten, particularmente para os Asquenazes, que também evitam o arroz. Muitos produtos kosher para o Pessach são isentos de cereais, não contendo glúten de todo. A fécula de batata é o principal produto utilizado como substituto. No entanto, consumir matzá só é obrigatório na primeira noite do Pessach e a lei judaica sustenta que ninguém deve colocar a sua saúde em risco apenas para cumprir um mandamento. Assim, a uma pessoa com doença celíaca grave não é permitido, muito menos exigido, que consuma outro matzá que não o isento de glúten, o qual é geralmente feito a partir de cevada.
Investigação
Estão a ser investigadas outras abordagens com o intuito de diminuir a necessidade de dieta, embora ainda estejam em fase de desenvolvimento e só é expectável que estejam disponíveis para a população em geral a longo prazo. A utilização de espécies de trigo geneticamente modificadas, ou espécies obtidas a partir de cultura seletiva, podem vir a permitir o consumo de trigo. No entanto, é possível que isto interfira com o efeito benéfico da gliadina na qualidade da farinha. Em alternativa, a exposição ao glúten pode ser minimizada pela ingestão de uma combinação de enzimas (propil endopeptidase e cisteíno protease) que degradam o peptídeo 33-mer no duodeno.
Entre os tratamentos alternativos que se encontram a ser investigados estão a inibição da zonulina, uma proteína sinalizadora endógena associada ao aumento da permeabilidade da parede intestinal, o que aumenta a apresentação da gliadina ao sistema imunitário. Estão também a ser investigados outros modificadores das fases melhor compreendidas da patogénese da doença celíaca, como a ação do HLA-DQ2 ou da transglutaminase tecidular e a interação MICA/NKG2D que pode estar envolvida na morte dos enterócitos.
História

A humanidade iniciou o cultivo de cereais durante o neolítico (início c. 9500 a.C.) no Crescente Fértil na Ásia ocidental, sendo improvável que a doença celíaca tivesse existido antes desta época. Areteu da Capadócia, que viveu na mesma região durante o século II, salientou a existência de uma síndrome de má absorção, com diarreia crónica e que provocava uma debilitação do corpo inteiro. Esta afeção "celíaca" (do grego κοιλιακός koiliakos, "abdominal") despertou o interesse da medicina ocidental quando foi apresentada uma tradução da obra de Areteu à Sydenham Society em 1856. O paciente descrito por Areteu apresentava dores de estômago e encontrava-se atrofiado, pálido, fraco e incapaz de trabalhar. A diarreia manifestava-se através de fezes líquidas esbranquiçadas, com mau cheiro e flatulência, sendo a doença intratável e de aparecimento recorrente. Areteu acreditava que a diarreia tinha origem na falta de calor no estômago, o qual seria necessário para digerir a comida, e numa diminuição da capacidade em distribuir os produtos da digestão pelo corpo. Registou ainda que esta doença afetava os idosos e principalmente as mulheres, excluindo explicitamente as crianças. A causa, de acordo com Areteu, podia ser outra doença crónica ou até mesmo a ingestão de quantidades copiosas de água fria.
O pediatra Samuel Gee fez a primeira descrição moderna da doença em crianças durante uma palestra no hospital pediátrico de Great Ormond Street em Londres em 1877. Gee conhecia as anteriores descrições e termos para a doença, tendo adotado o mesmo termo que Areteu (doença celíaca). Afirmou também que se o paciente puder ser curado, deverá ser através da dieta. Reconheceu ainda que a intolerância ao leite é um problema característico de crianças celíacas e que devem ser evitados alimentos ricos em amido. No entanto, também proibia o consumo de arroz, fruta e vegetais, os quais são seguros para consumo, e recomendava a ingestão de carne crua e fatias finas de pão torrado. Gee salientava o sucesso em particular de uma criança alimentada diariamente com mexilhões, embora a mesma criança não tivesse sido capaz de sustentar essa mesma dieta por mais do que uma estação.
Christian Archibald Herter, um médico norte-americano, escreveu em 1908 um livro sobre crianças com a doença celíaca, a qual designava por "infantilismo intestinal". Herter verificou atrasos no crescimento e que a gordura era melhor tolerada que os hidratos de carbono. O epónimo "doença de Gee-Herter" era por vezes utilizado em reconhecimento das suas contribuições. Sidney Haas, um pediatra norte-americano, descreveu em 1924 os benefícios de uma dieta à base de bananas em celíacos. Esta dieta continuou a ser popular até ser determinada a verdadeira causa da doença celíaca.
Embora se suspeitasse do papel dos hidratos de carbono, a associação da doença com o trigo só seria feita na década de 1940 pelo pediatra holandês Willem Karel Dicke. É provável que para esta descoberta tenha contribuído a melhoria dos seus pacientes durante a grande fome holandesa de 1944, durante a qual a farinha era escassa. Dicke reparou que a escassez de pão levou a que a taxa de mortalidade entre crianças celíacas tivesse diminuído drasticamente, desde mais de 35% até praticamente zero. Reportou também que a partir do momento em que o trigo voltou a estar disponível após a guerra, a taxa de mortalidade regressou aos números anteriores. A ligação com o glúten do trigo foi feita em 1952 por uma equipa de Birmingham, em Inglaterra. A atrofia das vilosidades do intestino foi descrita pelo médico britânico John W. Paulley em 1954, a partir de amostras recolhidas durante cirurgias, o que abriu caminho à recolha de amostras por endoscopia. Ao longo da década de 1960 foram descobertas novas características da doença. O seu caráter hereditário foi reconhecido em 1965. Em 1966, a dermatite herpetiforme foi associada à sensibilidade ao glúten.
Notas
Ligações externas
- «Federação das Associações de Celíacos do Brasil»
- «Associação Portuguesa de Celíacos»
- «Doença celíaca» - diretriz prática da Organização Mundial de Gastroenterologia
- Este artigo foi inicialmente traduzido, total ou parcialmente, do artigo da Wikipédia em inglês cujo título é «Coeliac disease».