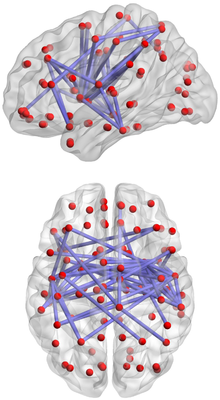
Redes neurais biológicas

Em neurociência, uma rede neural biológica é uma série de neurônios interconectados. O meio pelo qual os neurônios interagem com seus vizinhos normalmente consiste de vários terminais axônicos conectados via sinapses a dendritos de outros neurônios. Se a somatória dos sinais de entrada ultrapassa um certo nível crítico, o neurônio gera um potencial de ação (PA), que é propagado ao longo de seu axônio, sendo transmitido, via neurotransmissores químicos ou como um sinal elétrico, a outros neurônios.
Redes neurais biológicas inspiraram a conceituação de modelos de rede neural artificial.
Primeiros estudos
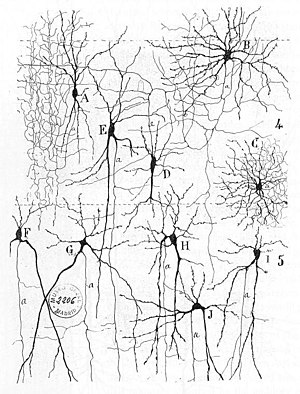
As primeiras descrições de redes neurais podem ser encontradas em Herbert Spencer - Principles of Psychology (1872), Theodor Meynert's - Psychiatry (1884), William James - Principles of Psychology (1890), e o projeto de Sigmund Freud para a psicologia científica (1895).
A primeira descrição de aprendizagem neuronal foi formulada por Hebb em 1949, em sua teoria hebbiana de aprendizagem. De acordo com esta teoria, o pareamento de atividade de neurônios pré e pós sinápticos pode afetar substancialmente a característica dinâmica dessas conexões e, portanto, facilitar ou inibir a transmissão de sinais. Os neurocientistas Warren Sturgis McCulloch e Walter Pitts publicaram os primeiros trabalhos sobre processamento de informações em redes neurais. Eles mostraram que, teoricamente, redes de neurônios artificiais poderiam implementar funções lógicas, aritméticas e simbólicas.
Modelos de neurônios simplificados foram, usualmente, chamados de perceptrons ou neurônios artificiais. Estes modelos simples explicam a somação neural (potenciais na membrana pós-sináptica que irão se somar no corpo celular). Modelos mais modernos explicam as transmissões sinápticas excitatórias e inibitórias caracterizando, em termos matemáticos, a biofísica de canais iônicos.
Conexões entre neurônios
As conexões entre neurônios são muito mais complexas do que aquelas implementadas em arquiteturas de redes neurais artificiais. Os tipos básicos de conexões entre neurônios são:
- Sinapse química, que é a sinapse mais comum, que consiste em um neurônio pré-sináptico liberando neurotransmissores, que são absorvidos pelo neurônio pós-sinaptico por receptores químicos, conhecidos como canais iônicos.
- Sinapse elétrica, transmite informação instantaneamente de uma célula para outra, com transferência direta de corrente elétrica entre a célula pré-sináptica e a pós-sináptica. Elas são particularmente úteis quando a velocidade e a precisão na transmissão do impulso são fundamentais, como, por exemplo, no músculo cardíaco e no músculo liso.
A transmissão sináptica pode ser excitatória ou inibitória, caso torne o neurônio pós-sináptico mais ou menos propenso a disparar um potencial de ação.
No nível eletrofisiológico, existem vários fenômenos que alteram as características de resposta das sinapses individuais (denominadas plasticidade sináptica) e os neurônios individuais (plasticidade intrínseca). Estes são frequentemente divididos em plasticidade de curto prazo e plasticidade a longo prazo. A plasticidade sináptica de longo prazo é frequentemente considerada o substrato de memória mais provável. Geralmente, o termo "neuroplasticidade" refere-se a mudanças no cérebro causadas por atividade ou experiência.
Conexões exibem características temporais e espaciais. As características temporais referem-se à eficácia da transmissão sináptica, dependente da atividade, continuamente modificada, denominada plasticidade sináptica dependente da espiga. Foi observado em vários estudos que a eficácia sináptica dessa transmissão pode sofrer aumento de curto prazo (chamado de facilitação) ou diminuição (depressão) de acordo com a atividade do neurônio pré-sináptico. A indução de mudanças a longo prazo na eficácia sináptica, por potenciação a longo prazo (LTP) ou depressão (LTD), depende fortemente do tempo relativo do início do potencial pós-sináptico excitatório e do potencial de ação pós-sináptica. A LTP é induzida por uma série de potenciais de ação que causam uma variedade de respostas bioquímicas. Eventualmente, as reações causam a expressão de novos receptores nas membranas celulares dos neurônios pós-sinápticos ou aumentam a eficácia dos receptores existentes.
Métodos de estudo
Diferentes técnicas de neuroimagem foram desenvolvidas para investigar a atividade das redes neurais. É comum o uso de "scanners cerebrais", ou neuroimagem funcional, para investigar a estrutura ou função do cérebro, seja simplesmente uma forma de avaliar melhor uma lesão cerebral com imagens de alta resolução, seja examinando as ativações relativas de diferentes áreas cerebrais. Tais tecnologias podem incluir fMRI (ressonância magnética funcional), PET (tomografia por emissão de pósitrons) e CAT (tomografia axial computadorizada). A neuroimagem funcional usa tecnologias de imagem específicas do cérebro para fazer varreduras do cérebro, geralmente quando uma pessoa está realizando uma tarefa específica, na tentativa de entender como a ativação de determinadas áreas do cérebro está relacionada à tarefa. Na neuroimagem funcional, especialmente fMRI, que mede a atividade hemodinâmica que está intimamente ligada à atividade neural, PET, e eletroencefalografia (EEG) é usado.
Modelos conexionistas servem como uma plataforma de teste para diferentes hipóteses de representação, processamento de informação e transmissão de sinal. Estudos de lesionamento em tais modelos, por exemplo, em redes neurais artificiais, nos quais partes dos nós são deliberadamente destruídos para ver como a rede funciona, também podem fornecer informações importantes no funcionamento de vários conjuntos de células. Da mesma forma, simulações de neurotransmissores disfuncionais em condições neurológicas (por exemplo, dopamina nos gânglios da base de pacientes com Parkinson) podem fornecer insights sobre os mecanismos subjacentes para os padrões de déficits cognitivos observados no grupo particular de pacientes. As previsões desses modelos podem ser testadas em pacientes ou através de manipulações farmacológicas, e esses estudos podem, por sua vez, ser usados para informar os modelos, tornando o processo interativo.